A Noncanonical mu-1A-Binding Motif in the N Terminus of HIV-1 Nef Determines Its Ability To Downregulate Major Histocompatibility Complex Class I in T LymphocytesSayuki Iijima, Young-Jung Lee, Hirotaka Ode, Stefan Arold, Nobuyuki Kimura, Masaru Yokoyama, Hironori Sato, Yasuhito Tanaka, Klaus Strebel, and Hirofumi Akari
HIV-1)は宿主免疫応答を特異的に制御することで、生体内において長期持続感染することが知られています。この機序として、HIV-1の調節蛋白の一つであるNef蛋白が抗原提示分子であるMHCクラスI(MHC-I)の発現抑制が報告されていましたが、その詳細な分子機構はこれまで未解明でした。本研究では、MHC-I発現制御に必須である、Nef蛋白と輸送蛋白の一つであるAP-1複合体mu-1Aサブユニットによる特異的結合に関する分子構造学的なメカニズムを明らかにすることに成功しました。この成果は、Nef蛋白を持つ霊長類免疫不全ウイルスの宿主免疫制御機構を解明した重要な発見であり、Journal
of Virology誌 2012年4月号に掲載されました。
掲載website: http://jvi.asm.org/content/86/7/3944.abstract
Journal of Virology 86, 3944-3951, 2012
Down-regulation of the major histocompatibility
complex class-I (MHC-I) by HIV-1 Nef protein is indispensable for evasion
of HIV-1 from protective immunity. Though it has been suggested that the
N-terminal region of Nef contributes to the function by associating with a
mu-1A subunit of adaptor protein-1, the structural basis of the
interaction between Nef and mu-1A remains elusive. We found that a
tripartite hydrophobic motif (Trp13/Val16/Met20) in the N-terminus of Nef
was required for the MHC-I down-regulation. Importantly, the motif
functioned as a non-canonical mu-1A-binding motif for the interaction with
the tyrosine motif-binding site of the mu-1A subunit. Our findings will
help understanding how HIV-1 evades the antiviral immune response by
selectively redirecting the cellular protein trafficking system.
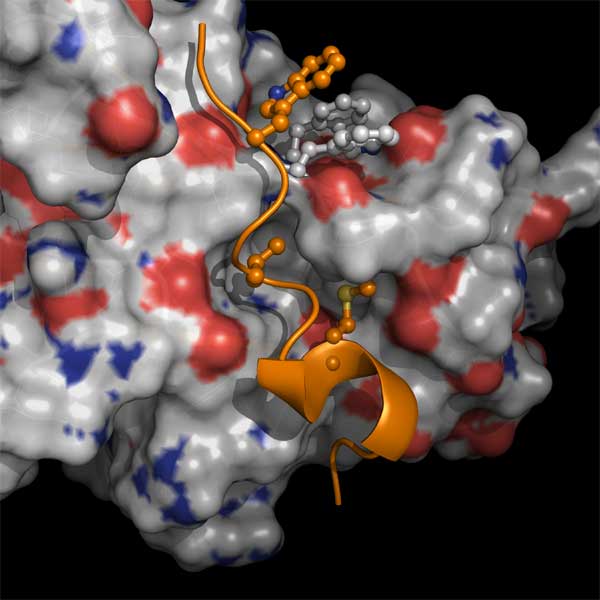
mu-1A分子(背景の雲様構造)とHIV-1 Nef蛋白N末端アミノ酸領域
(オレンジ色のリボン及びボール)の分子結合シミュレーション解析図
(大出裕高博士の提供による)
Interaction between a non-canonical mu-1A-binding motif
(Trp13/Val16/Met20) (orange ball and stick representation) of the
N-terminus of human immunodeficiency virus type 1 (HIV-1) Nef and the
tyrosine motif-binding site in a mu-1A subunit of adaptor protein-1
(surface representation). Trp13 in the Nef creates aromatic interactions
with Phe18 and Trp240 in the mu-1A (white ball and sticks), while side
chains of Val16 and Met20 are inserted into a cavity on the surface of the
mu-1A. The interaction is required for down-regulation of the major
histocompatibility complex class-I (MHC-I) and evasion of HIV-1 from
protective immunity. (provided by Dr. Hirotaka Ode)
MAR/13/2012
Copyright(C) 2012 PRI ( ). ).
| 






